Sciences Physiques pour enseignant du premier degré
Couleurs de la lumičre et longueur d'onde
Des lumičres invisibles
Couleur et température
Emission de lumičre par luminescence
Petit lexique : unités, niveau d'énergie, spectre
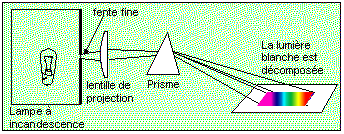
Un rayon de lumičre blanche émise par une lampe ŕ incandescence passant au
travers d'un prisme ou d'un réseau optique,est "étalé" en une
infinité de rayons de toutes les couleurs visibles, du rouge jusqu'au violet. La lumičre
blanche est l'addition de lumičres de toutes les couleurs.
Ainsi, l'arc en ciel, obtenu par la décomposition de la lumičre blanche du Soleil par le
prisme des gouttelettes d'eau est-il formé d'une infinité de couleurs visibles du rouge
au violet.
 |
La lumičre est descriptible par une onde lumineuse. Il existe une relation directe
entre la couleur de la lumičre et la longueur de l'onde lumineuse ; une onde rouge a une
longueur d'onde de 0,8 micromčtres, jaune 0,6 micromčtres, verte 0,55 micromčtres,
violette 0,4 micromčtres.
La lumičre visible n'est qu'une petite "fenętre" d'un phénomčne plus
général : les ondes électromagnétiques. Entre des longueurs d'onde de 0,4 et 0,8
micromčtres, la lumičre est visible, c'est ŕ dire que l'oeil humain transforme
l'énergie lumineuse reçue en influx nerveux.
Les longueurs d'onde plus courtes que 0,4 µm, sont le domaine des rayons
ultra-violets, puis des rayons X et des rayons gamma.
Les longueur d'onde plus grandes que 0,8 µm, celui des infra-rouges, des ondes millimétriques et des ondes radio.

Les récepteurs qui transforment l'énergie de l'onde électromagnétique en une autre forme d'énergie sont différents selon la
longueur d'onde ; antenne radio, capteurs infrarouge, oeil, plaque photographique etc.
De męme la transparence des substances dépend aussi de
la longueur d'onde ; chaque corps possčde une ou des "fenętres" de
transparence. Par exemple, certains gaz comme le dioxyde de carbone sont transparents ŕ la
lumičre visible (l compris entre 0,4 µm et 0,8 µm), mais
opaques pour les infra rouge "thermiques" (l plus
grand que 4 µm )
Il en est de męme pour l'absorbance ; certains corps seront de trés bon miroirs pour
certaines longueurs d'onde et trés absorbant pour d'autres.
La plupart des sources de lumičre sont chaudes ; elles émettent de
la lumičre par
incandescence. La lumičre émise est composée d'une plage étendue de
longueurs d'onde. La répartition énergétique des ondes émises selon
leur longueur d'onde ne dépend que de la température de la source.
Une source ŕ 20 °C (293 K) émet surtout des infra-rouge (maximum aux environ de 10 µm =10 .10-6m = 2,9 .10-3/293), une source ŕ 5450 °C (5723 K) émet de la lumičre visible avec un maximum ŕ 0,5 µm = 0,5 .10-6m = 2,9 .10-3/5273 (lumičre verte).
Ainsi, la lumičre émise par le Soleil (température de surface de 5700°C) est principalement constituée de lumičre
visible et de proche infra-rouge (l plus petit que 4 µm )
alors que la Terre (température de surface 20°C) émet plutot des infra rouge "thermiques" (l plus grand que 4 µm )
Une photo satellite en lumičre visible montre ce qui est réfléchie et
diffusé par la Terre et les nuages de l'éclairage du Soleil ; une photo
en infra rouge thermique, elle montre ce qui est émis par la surface de
la Terre.
Le corps humain, de surface 0,33 m2 ŕ 37°C soit 310 K emet une puissance de
0,33 * 5,69.10-8*(310)4 = 173 watts soit plus qu'une lampe ŕ
incandescence !... mais en infra-rouge l vers 10µm de longueur d'onde.
Les atomes et les molécules d'un corps peuvent absorber et réemettre de l'énergie si
la quantité absorbée et réémise correspond ŕ des saut de niveau énergétique (des
quantas).
Si l'énergie réémise est sous forme lumineuse, la fréquence de l'onde émise dépend
du "saut" d'énergie de l'atome émetteur.
DE= h * n
DE est la valeur du saut d'énergie (en joules) ; n est la fréquence de l'onde émise (en hertz)
sa longueur d'onde vaut alors l = c / n (c est la vitesse de la lumičre)
h est appelé constante de Planck et vaut 6,64 10 -34 J.s
Un corps qui émet de la lumičre de cette maničre n'émet qu'une série d'ondes électromagnétique de longueur d'ondes précise ; son spectre est constitué de raies lumineuses correspondant ŕ tous les sauts énergétiques que l'atome peut faire en émettant une onde lumineuse. Celui ci est en quelque sorte sa "signature" lumineuse.
| Dans l'exemple théorique ci-contre, l'atome peut se trouver sur un des
trois niveaux d'énergie possible ; s'il est excité il sautera sur un niveau supérieur et
redescendra sur un niveau inférieur en émettant une onde lumineuse correspondant au saut
d'énergie DE. La lumičre émise aura alors la longueur d'onde l=h.c/DE Cet atome émettra sur trois longueurs d'onde. 0,3 µm (ultra-violet) correspondant au saut de 3,95 eV ; 0,56 µm (vert) pour le saut de 2,21 eV et 0,71 µm (rouge) pour le saut de 3,95 - 2,21 = 1,74 eV Les énergies sont exprimées en électron-Volts ; 1 eV = 1,6 10 -19 J |
Les raies spectrales sont classées en trois séries ; celles dont le niveau d'arrivée est le niveau fondamental (série de Lyman surtout en UV) celle dont le niveau d'arrivée est le premier niveau (série de Balmer surtout en visible) et celle dont le niveau d'arrivée est le troisičme (série de Paschen surtout en IR)


Certaines lampes utilisées couramment combinent l'émission de lumičre par incandescence et par luminescence ; sur un fond spectral continu, se dégagent quelques raies de luminescence.
Les étoiles émettent principalement par incandescence ; mais les atomes présents dans leur atmosphčre, absorbent les longueurs d'onde correspondant ŕ leurs sauts d'énergie. Le spectre de la lumičre d'une étoile, est constitué d'un fond continu et de raies sombres d'absoprtion qui sont autant de "signatures" des atomes. On peut ainsi déterminer la température de leur surface et leur composition.
Spectre lumineux
répartition des ondes émises ou absorbée par une source en fonction de la longueur d'onde.